- 고온의 기체(단원자) 금속을 여러 개 묶어서 고체 금속을 만들 수 있습니다.
- 기체(단원자)와 고체 상태에서 방출하는 스펙트럼에는 어떤 차이가 있을까요?
- 위 시뮬레이션은 단순 예시이며, 실제 원자를 대표하지 않습니다.
선 스펙트럼
원자는 들어온 에너지를 흡수하고 주변에 그 에너지를 다시 방출할 수 있습니다. 단원자 분자나 금속 기체와 같은 단일 원자가 방출하는 에너지는 정해진 값만 가질 수 있습니다. 이것은 원자핵에 종속된 전자들이 띄엄띄엄하게 정해진 에너지만 가질 수 있기 때문입니다.
연속 스펙트럼
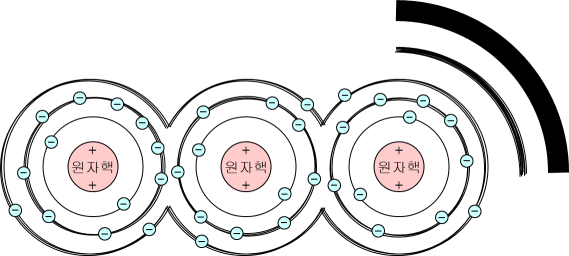
원자핵이 하나만 홀로 있다면 위와 같이 설명하고 끝이 나겠지만, 고체와 같이 원자핵들이 밀도 있게 붙어 있는 경우에는 원자들이 가진 전자 궤도들이 서로 포개지면서 두꺼워집니다.
그 결과 에너지 준위는 이제 하나의 선이 아니라 일정한 폭을 가진 띠(밴드)의 형태를 띠게 됩니다.
이렇게 두껍게 된 에너지 준위를 에너지 띠(energy band)라고 부르며, 띠와 띠 사이, 선과 띠 사이에서는 해당 에너지를 가지는 전자들이 존재할 수 없기 때문에 띠 간격(energy gap)이라고 부릅니다.
띠(밴드)가 형성되면 방출되는 에너지도 다양해지며, 일부 연속된 스펙트럼이 관찰되기 시작합니다.
예시: 저압 나트륨등(LPS Lamp)과 고압 나트륨등(HPS Lamp)
나트륨등은 진공 방전관 내부에 미량의 나트륨을 넣고 방전시켜 밝은 빛을 방출하는 기구입니다.
나트륨등은 내부 기체의 밀도에 따라서 저압(Low-Pressure) 나트륨등과 고압(High-Pressure) 나트륨등으로 나눌 수 있습니다.
저압 나트륨등은 금속 기체에 가깝기 때문에 방출되는 빛이 주로 590mm에 집중되는 경향을 보입니다. (나트륨의 불꽃 반응색과 같음)
반면, 고압 나트륨등은 원자들의 상호 간섭에 의해 연속 스펙트럼을 이루며 흰색에 가까워집니다.

저압 나트륨등. (2023, August 19). In Wikipedia. https://en.wikipedia.org/wiki/Sodium-vapor_lamp

고압 나트륨등. (2023, August 19). In Wikipedia. https://en.wikipedia.org/wiki/Sodium-vapor_lamp
실온의 고체 금속이 대부분 은색을 띠는 이유
대부분의 금속은 원자 구조 외곽에 대규모의 전자 띠를 가지고 있습니다(금속 결합). 그리고 자유 전자들이 띠에서 자유롭게 움직일 수 있습니다. 이 때문에 금속은 대부분의 가시광선 파장을 흡수할 수 있고, 그대로 다시 방출할 수 있습니다.